Gases: teoría cinético molecular |
La teoría cinética de los gases se enuncia en los siguientes postulados, teniendo en cuenta un gas ideal o perfecto:
1. Las sustancias están constituidas por moléculas pequeñísimas ubicadas a gran distancia entre sí; su volumen se considera despreciable en comparación con los espacios vacíos que hay entre ellas.
2. Las moléculas de un gas son totalmente independientes unas de otras, de modo que no existe atracción intermolecular alguna.
3. Las moléculas de un gas se encuentran en movimiento continuo, en forma desordenada; chocan entre sí y contra las paredes del recipiente, de modo que dan lugar a la presión del gas.
4. Los choques de las moléculas son elásticos, no hay pérdida ni ganancia de energía cinética, aunque puede existir transferencia de energía entre las moléculas que chocan.
5. La energía cinética media de las moléculas es directamente proporcional a la temperatura absoluta del gas; se considera nula en el cero absoluto.
Los gases reales existen, tienen volumen y fuerzas de atracción entre sus moléculas. Además, pueden tener comportamiento de gases ideales en determinadas condiciones: temperaturas altas y presiones muy bajas
Modelo corpuscular
De acuerdo con los postulados enunciados, podemos hacernos una imagen clara y concisa del modelo que represente el comportamiento de un gas.
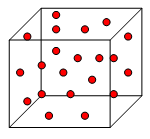
Dicho modelo, debe ser el más elemental posible, debe explicar las propiedades observadas en los gases, debe contemplar la existencia de partículas muy pequeñas, de tamaño despreciable frente al volumen total, dotadas de grandes velocidades en constante movimiento caótico, chocando entre sí o con las paredes del recipiente. En cada choque se supone que no hay pérdida de energía y que no existe ningún tipo de unión entre las partículas que forman el gas.
|
|
Un modelo corpuscular para gases
|
Así, el concepto de presión , estará ligado al de los choques de las partículas sobre las paredes, debido al movimiento que llevan, presión que se ejerce sobre todas las direcciones, no existiendo direcciones privilegiadas. Así, cuantos más choques se produzcan, mayor es la presión del gas.
La temperatura , indicará la energía cinética media de las partículas: si la temperatura de un gas es superior a otro, sus partículas por término medio, poseen mayor velocidad.
Fuente Internet:
http://www.cespro.com/Materias/MatContenidos/Contquimica/QUIMICA_INORGANICA/gases.htm

