Carbono |
Descripción
|
Nombre |
Carbono |
|
Número atómico |
6 |
|
Valencia |
2,+4,-4 |
|
Configuración electrónica |
1s 2 2s 2 2p 2 |
|
Masa atómica (g/mol) |
12,01115 |
|
Densidad (g/ml) |
2,26 |
|
Punto de ebullición (ºC) |
4830 |
|
Punto de fusión (ºC) |
3727 |
|
Descubridor |
Los antiguos |
Carbono, de símbolo C, es un elemento crucial para la existencia de los organismos vivos, y que tiene muchas aplicaciones industriales importantes. Su número atómico es 6; y pertenece al grupo 14 (o IV A) del sistema periódico.
Propiedades
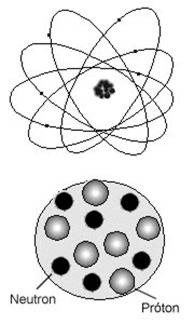
|
| Átomo de carbono. |
Las propiedades físicas y químicas del carbono dependen de la estructura cristalina del elemento.
Un gran número de metales se combinan con el elemento a temperaturas elevadas para formar carburos.
Con el oxígeno forma tres compuestos gaseosos: monóxido de carbono, CO, dióxido de carbono, CO 2 , y subóxido de carbono, C 3 O 2 .
Los dos primeros son los más importantes desde el punto de vista industrial.
El carbono es un elemento único en la química porque forma un número de compuestos mayor que la suma total de todos los otros elementos combinados.
El grupo más grande de estos compuestos es el constituido por carbono e hidrógeno . Se estima que se conoce un mínimo de 1.000.000 de compuestos orgánicos y este número crece rápidamente cada año. Aunque la clasificación no es rigurosa, el carbono forma otra serie de compuestos considerados como inorgánicos, en un número mucho menor al de los orgánicos.
Las tres formas de carbono elemental existentes en la naturaleza (diamante, grafito y carbono amorfo) son sólidos con puntos de fusión extremadamente altos, e insolubles en todos los disolventes a temperaturas ordinarias. Las propiedades físicas de las tres formas difieren considerablemente a causa de las diferencias en su estructura cristalina.
En el diamante, el material más duro que se conoce, cada átomo está unido a otros cuatro en una estructura tridimensional, mientras que el grafito consiste en láminas débilmente unidas de átomos dispuestos en hexágonos.
El carbono químicamente puro se prepara por descomposición térmica del azúcar (sacarosa) en ausencia de aire.
El carbono tiene la capacidad única de enlazarse con otros átomos de carbono para formar compuestos en cadena y cíclicos muy complejos. Esta propiedad conduce a un número casi infinito de compuestos de carbono, siendo los más comunes los que contienen carbono e hidrógeno.

|
| Pieza de carbono. |
Sus primeros compuestos fueron identificados a principios del siglo XIX en la materia viva, y, debido a eso, el estudio de los compuestos de carbono se denominó química orgánica .
A temperaturas normales, el carbono se caracteriza por su baja reactividad. A altas temperaturas, reacciona directamente con la mayoría de los metales formando carburos, y con el oxígeno formando monóxido de carbono (CO) y dióxido de carbono (CO 2 ).
El carbono en forma de coque se utiliza para eliminar el oxígeno de las menas que contienen óxidos de metales, obteniendo así el metal puro. El carbono forma también compuestos con la mayoría de los elementos no metálicos, aunque algunos de esos compuestos, como el tetracloruro de carbono (CCl 4 ), han de ser obtenidos indirectamente.
Estado natural
El carbono es un elemento ampliamente distribuido en la naturaleza, aunque sólo constituye un 0,025% de la corteza terrestre, donde existe principalmente en forma de carbonatos.
Varios minerales, como caliza, dolomita, yeso y mármol, tienen carbonatos.
Todas las plantas y animales vivos están formados de compuestos orgánicos complejos en donde el carbono está combinado con hidrógeno, oxígeno, nitrógeno y otros elementos.
Los vestigios de plantas y animales vivos forman depósitos: de petróleo, asfalto y betún. Los depósitos de gas natural contienen compuestos formados por carbono e hidrógeno.
El elemento libre tiene muchos usos, que incluyen desde las aplicaciones ornamentales del diamante en joyería hasta el pigmento de negro de humo en llantas de automóvil y tintas de imprenta.
Otra forma del carbono, el grafito, se utiliza para crisoles de alta temperatura, electrodos de celda seca y de arco de luz, como puntillas de lápiz y como lubricante. El carbón vegetal, una forma amorfa del carbono, se utiliza como absorbente de gases y agente decolorante.
Los compuestos de carbono tienen muchos usos.

|
| Diamante. |
El dióxido de carbono se utiliza en la carbonatación de bebidas, en extintores de fuego y, en estado sólido, como enfriador (hielo seco). El monóxido de carbono se utiliza como agente reductor en muchos procesos metalúrgicos. El tetracloruro de carbono y el disulfuro de carbono son disolventes industriales importantes. El freón se utiliza en aparatos de refrigeración. El carburo de calcio se emplea para preparar acetileno; es útil para soldar y cortar metales, así como para preparar otros compuestos orgánicos. Otros carburos metálicos tienen usos importantes como refractarios y como cortadores de metal.
El dióxido de carbono es un componente importante de la atmósfera y la principal fuente de carbono que se incorpora a la materia viva. Por medio de la fotosíntesis, los vegetales convierten el dióxido de carbono en compuestos orgánicos de carbono, que posteriormente son consumidos por otros organismos.
Ver: Ciclo del carbono
El carbono amorfo se encuentra con distintos grados de pureza en el carbón de leña, el carbón, el coque, el negro de carbono y el negro de humo.
El negro de humo, al que a veces se denomina de forma incorrecta negro de carbono, se obtiene quemando hidrocarburos líquidos como el queroseno, con una cantidad de aire insuficiente, produciendo una llama humeante. El humo u hollín se recoge en una cámara separada. Durante mucho tiempo se utilizó el negro de humo como pigmento negro en tintas y pinturas, pero ha sido sustituido por el negro de carbono, que está compuesto por partículas más finas.
El negro de carbono, llamado también negro de gas, se obtiene por la combustión incompleta del gas natural y se utiliza sobre todo como agente de relleno y de refuerzo en el caucho o hule.
En 1985, los científicos volatilizaron el grafito para producir una forma estable de molécula de carbono consistente en 60 átomos de carbono dispuestos en una forma esférica desigual parecida a un balón de fútbol. La molécula recibió el nombre de buckminsterfulereno ('pelota de Bucky' para acortar) en honor a R. Buckminster Fuller, el inventor de la cúpula geodésica. La molécula podría ser común en el polvo interestelar.
Aplicaciones científicas
El isótopo del carbono más común es el carbono 12; en 1961 se eligió este isótopo para sustituir al isótopo oxígeno 16 como medida patrón para las masas atómicas, y se le asignó la masa atómica 12.
Los isótopos carbono 13 y carbono 14 se usan como trazadores (consultar Trazador isotópico) en la investigación bioquímica. El carbono 14 se utiliza también en la técnica llamada método del carbono 14 , que permite estimar la edad de los fósiles y otras materias orgánicas. Este isótopo es producido continuamente en la atmósfera por los rayos cósmicos, y se incorpora a toda la materia viva.
Como el carbono 14 se desintegra con un periodo de semidesintegración de 5.760 años, la proporción entre el carbono 14 y el carbono 12 en un espécimen dado, proporciona una medida de su edad aproximada.
Configuración electrónica
El átomo de carbono constituye el elemento esencial de toda la química orgánica, y debido a que las propiedades químicas de elementos y compuestos son consecuencia de las características electrónicas de sus átomos y de sus moléculas, es necesario considerar la configuración electrónica del átomo de carbono para poder comprender su singular comportamiento químico.
Se trata del elemento de número atómico Z = 6. Por tal motivo su configuración electrónica en el estado fundamental o no excitado es 1s 2 2s 2 2p 2 . La existencia de cuatro electrones en la última capa sugiere la posibilidad bien de ganar otros cuatro convirtiéndose en el ion C 4- cuya configuración electrónica coincide con la del gas noble Ne, bien de perderlos pasando a ion C 4+ de configuración electrónica idéntica a la del He.
En realidad una pérdida o ganancia de un número tan elevado de electrones indica una dosis de energía elevada, y el átomo de carbono opta por compartir sus cuatro electrones externos con otros átomos mediante enlaces covalentes. Esa cuádruple posibilidad de enlace que presenta el átomo de carbono se denomina tetravalencia.
El carbono frente al silicio
Cabe preguntarse si la situación del carbono es singular o si por el contrario algún otro elemento participa de sus mismas propiedades. Observando el sistema periódico se advierte que el silicio está situado en el mismo grupo justo debajo del carbono y con idéntica configuración electrónica externa.
¿Por qué razón la vida se ha desarrollado sobre los compuestos del carbono y no sobre los del silicio? ¿Por qué los derivados del silicio son tan poco numerosos frente a los del carbono?
La existencia en el silicio de ocho electrones internos adicionales respecto del carbono hace que los electrones externos o de valencia responsables del enlace químico estén más alejados del núcleo y, por tanto, atraídos por él más débilmente. Ello se traduce en que la fuerza de los enlaces del silicio es comparativamente menor; particularmente lo es el enlace Si-Si, lo que le convierte en más reactivo, es decir, menos estable químicamente.
No obstante, el silicio cristaliza formando una red tridimensional semejante a la del diamante, y sus derivados constituyen el 87 % de la composición de la corteza terrestre. Su combinación con el oxígeno origina la sílice o cuarzo (SiO 2 ). El carácter francamente polar de esta unión da lugar a estructuras reticulares o redes cristalinas que por sus propiedades se parecen enormemente a las de los sólidos iónicos.
La química de compuestos del carbono
El átomo de carbono, debido a su configuración electrónica, presenta una importante capacidad de combinación. Los átomos de carbono pueden unirse entre sí formando estructuras complejas y enlazarse a átomos o grupos de átomos que confieren a las moléculas resultantes propiedades específicas. (Ver: Grupos funcionales )
La enorme diversidad en los compuestos del carbono hace de su estudio químico una importante área del conocimiento puro y aplicado de la ciencia actual.
Durante mucho tiempo la materia constitutiva de los seres vivos estuvo rodeada de no pocas incógnitas. Frente a la materia mineral presentaba, entre otras, una característica singular, su capacidad de combustión. Parecía como si los únicos productos capaces de arder hubieran de proceder de la materia viviente.
En los albores de la química como ciencia se advirtió, además, que si bien la materia procedente de organismos vivos podía degradarse en materia mineral por combustión u otros procesos químicos, no era posible de ninguna manera llevar a cabo en el laboratorio el proceso inverso.
Argumentos de este estilo llevaron a Berzelius, a comienzos del siglo XIX, a sugerir la existencia de dos tipos de materia en la naturaleza, la materia orgánica o materia propia de los seres vivos, y la materia inorgánica.
Para justificar las diferencias entre ambas se admitió que la materia orgánica poseía una composición especial y que su formación era debida a la intervención de una influencia singular o «fuerza vital» exclusiva de los seres vivos y cuya manipulación no era posible en el laboratorio.
La crisis de este planteamiento, denominado vitalismo, llevó consigo el rápido desarrollo de la química de la materia orgánica en los laboratorios, al margen de esa supuesta «fuerza vital».
En la actualidad, superada ya la vieja clasificación de Berzelius, se denomina química orgánica a la química de los derivados del carbono e incluye el estudio de los compuestos en los que dicho elemento constituye una parte esencial, aunque muchos de ellos no tengan relación alguna con la materia viviente.
HIDROCARBUROS: ASPECTOS ESTRUCTURALES
La geometría de sus moléculas.
Los hidrocarburos son los derivados del carbono más sencillos. Resultan de la unión únicamente de átomos de carbono con átomos de hidrógeno y de átomos de carbono entre sí formando cadenas que pueden ser abiertas o cerradas y cuyos «eslabones» pueden estar unidos por enlaces simples o por enlaces múltiples. Aquellos hidrocarburos que presentan únicamente enlaces simples reciben el nombre de hidrocarburos saturados (alcanos).
El representante más sencillo de los hidrocarburos saturados es el metano CH 4 ; no obstante, el etano C 2 H 6 da una mejor idea de las características de este tipo de hidrocarburos.
|
|
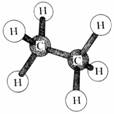
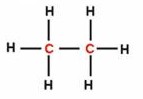
| Etano (un enlace carbono-carbono). | |
La molécula de etano está compuesta por dos átomos de carbono y seis átomos de hidrógeno que se unen entre sí mediante enlaces covalentes sencillos. Desde un punto de vista puramente geométrico se puede representar la molécula de etano mediante dos tetraedros contiguos y opuestos por uno de sus vértices, en donde los dos átomos de carbono ocupan los centros de los respectivos tetraedros, y los de hidrógeno los vértices libres.
|
|
| Eteno, dos carbonos con enlace doble. |
Los hidrocarburos no saturados se caracterizan, desde el punto de vista de su estructura molecular, por la presencia de enlaces dobles (alquenos) o triples (alquinos). La molécula de eteno o etileno está formada por dos átomos de carbono unidos por un enlace doble; mediante sus otros dos enlaces restantes cada átomo de carbono se une a otros tantos átomos de hidrógeno.
Efectos del Carbono sobre la salud
El carbono elemental es de una toxicidad muy baja. Los datos presentados aquí de peligros para la salud están basados en la exposición al negro de carbono, no carbono elemental. La inhalación continuada de negro de carbón puede resultar en daños temporales o permanentes a los pulmones y el corazón.
Se ha encontrado pneumoconiosis en trabajadores relacionados con la producción de negro de carbón. También se ha dado parte de afecciones cutáneas tales como inflamación de los folículos pilosos, y lesiones de la mucosa bucal debidos a la exposición cutánea.
Carcinogenicidad: El negro de carbón ha sido incluido en la lista de la Agencia Internacional de Investigación del Cáncer (AIIC) dentro del grupo 3 (agente no clasificable con respecto a su carcinogenicidad en humanos).
Efectos ambientales del Carbono
No se tiene constancia de que el carbono tenga efectos negativos sobre el medio ambiente.
Ver: Ciclo del carbono
Fuentes Internet:
http://www.lafacu.com/apuntes/quimica/comp_carb/default.htm
http://www.lenntech.com/espanol/tabla-peiodica/C.htm

