Función química |
Entendido ya lo que son los grupos funcionales , veremos cuáles son las principales funciones químicas (definidas por los grupos funcionales).
Recordemos:
Cada grupo funcional determina las propiedades químicas de las sustancias que los poseen; es decir, determina su función química .
Entonces, se llama función química a las propiedades comunes que caracterizan a un grupo de sustancias que tienen estructura semejante; es decir, que poseen un determinado grupo funcional.
Existen funciones en la química inorgánica y en la química orgánica y para comprender el término función podemos hacer una analogía con el concepto de familia.
En una familia hay rasgos característicos que identifican a sus miembros, de la misma manera se podría afirmar que en las sustancias, tanto orgánicas como inorgánicas, existen agrupaciones de átomos, o grupo funcional , que debido a sus características comunes poseen un comportamiento típico.
Si nos referimos a las funciones en química inorgánica , se pueden distinguir cinco grandes familias, las cuales poseen ramificaciones filiales y que se organizan de la siguiente manera:
1.- Óxidos : ( Ácidos, Básicos, Neutros, Peròxidos y Superóxidos ).
2.- Hidróxidos.
3.- Ácidos : ( Hidrácidos y Oxácidos ).
4.- Sales : ( Haloideas y Oxisales (Neutras, Ácidas, Básicas y Dobles)).
5.- Hidruros: Metálicos y no Metálicos.
En tanto las funciones de la química orgánica son muchas más, destacándose entre todas la función hidrocarburo , porque de ella se desprenden todas las demás.
En química orgánica, dependiendo de si el grupo funcional característico posee átomos de oxígeno, de nitrógeno o es algún halógeno, la función química será oxigenada, nitrogenada o halogenada .
Las funciones químicas más importantes son:
|
Oxigenadas |
Nitrogenadas |
Halogenadas |
|
Alcoholes |
Aminas |
Derivados halogenados |
|
Éteres |
Amidas |
|
|
Aldehídos |
Nitrilos |
|
|
Cetonas |
|
|
|
Acido carboxílico |
|
|
|
Esteres |
|
|
|
|
|
|
|
|
|
|
Alcoholes
Cualquier compuesto orgánico que mediante un enlace sencillo incluya el grupo funcional –OH (hidroxilo) en su estructura molecular pertenece a la función química alcoholes.
(Ver: PSU: Química, Pregunta 08_2005)
Igual como la mayoría de los compuestos orgánicos, un alcohol puede contener más de un grupo –OH en su molécula.
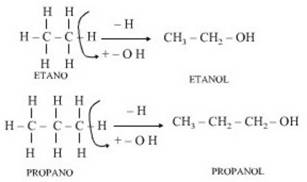
En la figura siguiente tenemos dos alcoholes, formados por la sustitución de un átomo de hidrógeno por un –OH en las moléculas de etano y de propano, para formar etanol y propanol , respectivamente.
|
Los alcoholes más simples se nombran manteniendo el nombre del alcano de origen , cambiando solo la última letra por la terminación “ol” : metano hace metanol; etano, hace etanol; propano hace propanol; butano hace butanol, etc.
El metanol (CH 3 – OH) es un líquido incoloro, de olor agradable, menos denso que el agua, muy tóxico, que puede producir ceguera si se ingiere un solo trago o puede producir la muerte en dosis mayores. Conocido también como el alcohol de la madera pues antiguamente se obtenía por la destilación de ese material. Se emplea como disolvente de pinturas y barnices, como anticongelante o como combustible en autos de carrera.
El alcohol etílico, también tóxico, aunque en menor grado que el metano, es el componente de los licores, y puede obtenerse por fermentación de frutas.
El nombre que recibe depende del origen de los azúcares fermentados: se llama ron , si procede del azúicar de caña; brandy , si es de la uva; tequila si se obtiene de agave; whisky si se destila de cebada o vodka si procede del centeno.
En la industria, el etanol se emplea como disolvente de grasas y resinas; en la vida doméstica se usa como antiséptico bajo la foirma de alcohol desnaturalizado (mezclado con sustancias que lo hacemn no ingerible).
Otro alcohol de uso frecuente en el hogar es el 2-propanol o isopropanol .
|
|
| 2-propanol o isopropanol |
Este producto orgánico se suele untar sobre la piel de un enfermo para “bajar la fiebre”; el calor del cuerpo humano produce la rápida evaporación de este alcohol y con ello baja la temperatura.
En la industria se le emplea como disolvente en la preparación de cremas y perfumes debido a que es muy soluble en agua.
Éteres
Se llaman éteres los compuestos formados por dos radicales unidos entre sí, mediante enlaces sencillos , a un átomo de oxígeno (O) . El grupo funcional es R – O – R (alcoxi) . Los radicales ( R ) que se unen al oxígeno pueden ser iguales o diferentes.
Para nombrarlos, se antepone la palabra éter al nombre de los radicales; si éstos son iguales se menciona el radical anteponiendo el prefijo “di” y agregando la terminación “ico” ; si los radicales son diferentes se nombra en primer lugar el de cadena más corta más el nombre del otro al que se le añade la misma terminación “ico” .
Algunos ejemplos de éteres son:
CH 3 – CH 2 – O – CH 2 – CH 3 éter dimetílico (los dos radicales son iguales)
CH 3 - O – CH 2 - CH 3 éter metiletílico (radicales distintos)
CH 3 – CH 2 – O – CH 2 – CH 2 - CH 3 éter propílico
El éter más conocido es el éter dietílico , que es un líquido muy volátil y un combustible poderoso, conocido porque sirve para “adormecer”. Desde mediados del siglo XIX se usó como anestésico por su fácil aplicación y porque no altera el pulso cardíaco
En la industria su uso más común es como solvente. Algunos son característicos por sus olores. Y se encuentran en las frutas siendo responsables de sus aromas. El olor del plátano, por ejemplo, se debe al éter metil pentílico .
Diversos éteres se emplean en la industria de los desodorantes y los jabones.
Aldehídos y cetonas
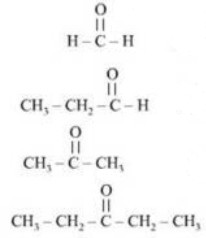
Son dos tipos de compuestos que en su molécula contienen al grupo funcional carbonilo ( >C=O, un átomo de oxígeno unido a uno de carbono por medio de un enlace doble ). Como ya dijimos anteriormente, si el grupo funcional es terminal (está al final de la cadena) se llaman aldehídos y se llamarán cetonas si el grupo funcional –C=O está unido a un átomo intermedio dentro de la cadena.
Debemos notar que apara los aldehídos, el grupo funcional incluye también al átomo de hidrógeno, por lo que el grupo queda como –CH=O .
Aldehído es una palabra compuesta que significa alcohol deshidrogenado, y para nombrar estos compuestos se cambia la terminación “ol” del alcohol por “al” que identifica a los aldehídos. Las cetonas, en cambio cambian la “ol” del alcohol por la terminación “ona” de la cetona.
El más común de los aldehídos es el metanal , conocido como formol, aldehído fórmico o formaldehído . Es un gas incoloro de olor penetrante y soluble en agua, en alcohol y en éter. Sus usos más comunes son para la conservación de órganos o partes anatómicas. También se usa como desinfectante. En la industria se usa para fabricar resinas, colorantes, germicidas y fertilizantes. Aldehídos de origen vegetal se añaden a ciertos productos para agregarles olor y sabor.
Otro aldehído es el propanal , que consta de tres carbonos y un grupo funcional carbonilo. El carbono del aldehído está unido al oxígeno por un doble enlace. Está también unido a un hidrógeno.
Importante:
Recuerde que en los aldehídos y las cetonas el enlace entre un carbono y el oxígeno es doble, por lo tanto disminuye el número de hidrógenos necesarios.
(Ver: PSU: Química, Pregunta 08_2005 )
|
Propanol
Propanona 3-Pentanona |
| Ejemplos de aldehídos y cetonas. |
La cetona más importante es la
propanona
o dimetil cetona
, conocida como acetona y se emplea para disolver barnices y lacas. La acetona es un líquido incoloro, inflamable, soluble en agua y de olor penetrante.
Ácidos carboxílicos
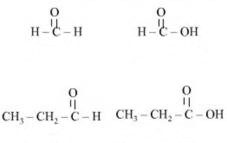
Compuestos orgánicos que en su molécula contienen el grupo funcional –COOH (un grupo con enlace =O y un grupo con enlace –OH , unidos al mismo átomo de carbono) son llamados ácidos carboxílicos o ácidos orgánicos . Estos compuestos se forman cuando el hidrógeno de un grupo aldehído es reemplazado por un grupo –OH, como vemos en las siguientes fórmulas estructurales, donde el metanal se convierte en ácido metanoico y el propanal se convierte en ácido propanoico :
| Metanal Ácido metanoico |
|
| Propanal Ácido propanoico |
| Generación de ácidos a partir de aldehídos. |
Para nombrar estos compuestos se antepone la palabra
“ácido”
seguida del nombre del alcano del que proviene y se añade la terminación
“ico”
.
Muchos de los ácidos carboxílicos, en especial aquellos que tienen entre cuatro y veinte átomos de carbono (siempre un número par) se encuentran en las grasas vegetales y animales y son llamados ácidos grasos saturados .
Ácidos carboxílicos con menos de cuatro átomos de carbono son líquidos y solubles en agua.
Aminas y amidas
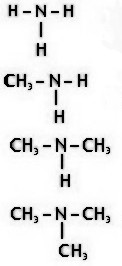
Las aminas son compuestos orgánicos derivados del amoniaco (NH 3 ) . Se forman cuando uno, dos o los tres átomos de hidrógeno se sustituyen por radicales, como vemos en la figura siguiente:
|
Metilamina
Dimetilamina
Trimetilamina |
| Aminas formadas por sustitución de hidrógenos (H) del amoníaco (NH 3 ) por radicales (CH 3 ). |
Para nombrar las aminas se nombran los radicales, empezando por el más simple y agregando al final la terminación
“amina”
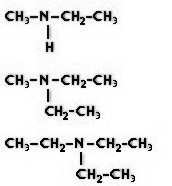
. En la figura de abajo, algunos ejemplos:
|
Metildietilamina Trietilamina |
| Fórmulas semidesarrolladas y el nombre de algunas aminas. |
Respecto a las
amidas
, son compuestos que
incluyen los grupos funcionales de aminas y ácidos carboxílicos
, como podemos ver en la figura siguiente:
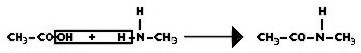
|
| Ácido etanoico Metilamina N - metiletanamida |
| Amidas, compuestos derivados de la combinación de aminas y ácidos carboxílicos. |
En todas las proteínas, tanto animales como vegetales, el grupo amida se encuentra repetido miles de veces en forma de cadenas, y también en algunas macromoléculas como el nylon.
Fuentes Internet:
http://nomenclatura_quimica.espacioblog.com/post/2007/04/28/funcion_quimica-2
http://www.visionlearning.com/library/module_viewer.php?mid=60&l=s
http://www.scribd.com/doc/9344616/Grupos-Funcionales-1
http://es.wikipedia.org/wiki/Enlace_carbono-ox%C3%ADgeno


 Metanal, formaldehído
Metanal, formaldehído
 Amoníaco
Amoníaco
 Metiletilamina
Metiletilamina